
이 글은 위의 책을 재구성한 내용입니다. (순서는 동일합니다)
활동전위의 성질
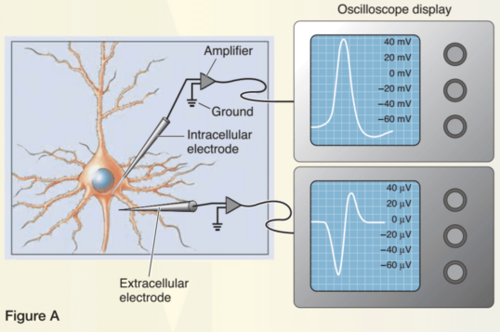
1. 세포 내 기록(intracellular recording)
- 세포 내 전극과 뉴런을 담그고 있는 용액에 놓인 전극(접지 전극) 사이의 전위차를 측정하는 방법
- 처음엔 막전위를 보이다가 활동전위가 도달하면 전위차가 양수가 되었다가 다시 돌아옴
2. 세포 외 기록(extracellular recording)
- 뉴런 근처의 세포 외 전극과 접지 전극 사이의 전위차를 측정하는 방법
- 처음엔 전위차가 0이다가 활동전위가 도달하면 양전하가 기록전극으로부터 뉴런으로 흐르고, 활동전위가 지나가면 양전하는 막을 지나 기록전극으로 다시 흐름
- rising phase: 세포막이 빠르게 탈분극되는 구간 (막전위가 약 40mV에 다다를 때까지 지속)
- overshoot: 세포막 내부가 외부에 비해 양전하를 가지는 구간
- falling phase: 활동전위가 빠르게 재분극되어 휴지 막전위보다 낮아질 때까지 떨어지는 구간
- undershoot: 과분극되는 구간 (이 하나의 활동전위 과정이 지속되는 데 2ms 소요)
- 활동전위의 발화빈도(firing frequency)는 탈분극 전류의 세기를 반영함
- 탈분극 전류의 세기가 증가함에 따라 발화빈도도 증가하지만, 최대 약 1000Hz 정도까지만 증가함
- 따라서, 활동전위 시작 후 최소 1ms 동안은 다른 활동전위 발생 불가 (절대불응기[absolute refractory period])
- 또한, 절대불응기 끝난 뒤에도 수 ms 동안은 새로 활동전위 생기기 힘듦 (상대불응기[relative refractory period])
- 역치가 평상시보다 높게 됨
- 광유전학(optogenetics)
- 박테리오돕신(bacteriorhodopsin)1은 빛을 받으면 H+을 세포 밖으로 내보내는 채널
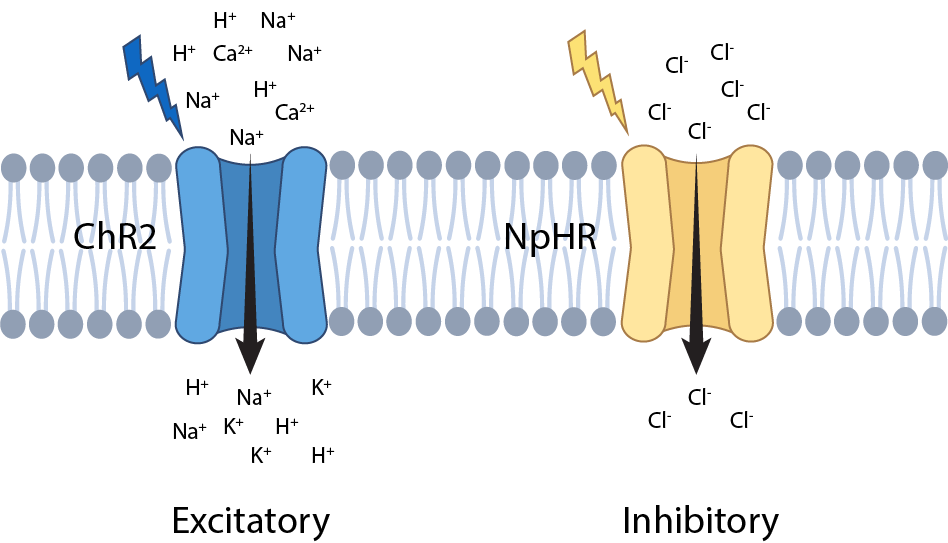
- 할로로돕신(halorhodopsin, NpHR)은 노란 빛(580nm)에 반응해 열리는 Cl-에 투과성이 있는 채널
- 채널로돕신2(channelrhodopsin 2, ChR2)는 파란 빛(460nm)에 반응해 열리는 Na+과 K+에 투과성이 있는 채널
- 위의 두 로돕신은 세포 내부가 더 음전하가 되게 해 신경활동을 억제하고, 채널로돕신은 세포 내부에 양전하를 갖고 와 신경활동을 유도함
활동전위: 이론
(1) 휴지기에는 gK(열린 K+ 채널 수)가 훨씬 많고, K+가 많이 왔다갔다하며 Vm = EK 유지
(2) 탈분극되면 gNa(열린 Na+ 채널 수)가 훨씬 많아지고, Na+가 세포막 내부로 유입되며 Vm이 ENa에 가까워짐
(3) 재분극이 되며 다시 gK가 많이 늘어나고, 세포막 외부로 K+가 많이 방출되며 Vm이 다시 EK 쪽으로 균형을 잡아감
(4) 휴지기로 돌아오며 Vm = EK가 되고, 다시 (1)과 같은 형태가 됨
활동전위: 실제
- 기본적인 메커니즘은 이론과 유사함 (상승기 동안 gNa 증가하고, 하강기에는 gK 증가하여 다시 음전하로 되돌림)
- 전압개폐성 Na+ 채널(voltage-gated sodium channel): 막전위에 따라 Na+를 선택적으로 통과시키는 통로
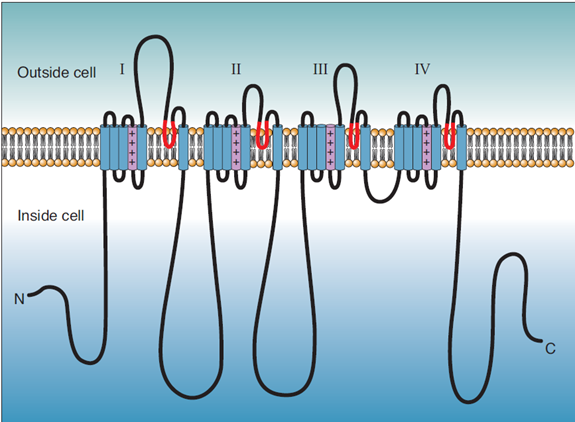
- 긴 폴리펩타이드 하나로 구성되어 있고, 이 단백질은 I에서 IV번까지 4개 도메인으로 구성되어 있음
- 각 도메인은 S1-S6까지 6개의 막관통성 알파 나선(transmembrane alpha helix)으로 구성되어 있음
- 4개의 도메인은 서로 뭉쳐서 가운데에 구멍을 형성
- 이 구멍은 막전위가 음의 값일 땐 닫혀 있다가 역치 이상으로 탈분극되면 Na+를 통과시킬 수 있도록 열림
- 이렇게 구멍고리들이 모여 형성된 선택필터(selectivity filter)는 Na+를 K+에 비해 12배나 잘 통과시킴 (hydrated Na+ 이온이 hydrated K+ 이온보다 작음)

- 이온 주위의 물 분자들(hydrated)은 selectivity filter를 통과할 수 있게 해줌 (결과적으로 Na+만 통과하게 하고, K+는 통과하지 못하게 함)
- Na+ 채널은 S4 구역(segment)에 전압센서가 존재하는데, 이 구역에는 양전하를 띠는 아미노산 잔기(residue)들이 나선의 코일을 따라 규칙적으로 배열되어 있음
- 막전위가 바뀌면 이들은 힘을 받아 구조적으로 변형되며 구멍이 열리는 것
- 특징
1. 채널이 열리기까지 짧은 지연시간이 있음 (역치까지 기다림)
2. 막전위가 -65mV에서 -40mV로 변했을 때 이온 채널이 열림 (그 전까지는 안 열림, 역치)
3. 이온 채널은 1ms 동안 열리고, 이후에는 비활성화되어 닫힘 (단백질의 구형 부분이 구멍을 막음)
4. 이후, 막전위가 역치 근처까지 낮아지기 전까진 탈분극이 되어도 이온 채널이 다시 열리지 않음 (절대불응기)
- Na+ 채널에 대한 독성물질의 효과
- 테트로도톡신(TTX)2, 색시톡신(saxitoxin)3: Na+ 채널 세포 바깥부분에 단단하게 결합하여 Na+의 통과 막음
- 바트라코톡신(batrachotoxin), 베라트리딘(veratridine), 아코니틴(aconitine): 이온 채널을 정상보다 낮은 막전위에서 열리게 하고 더 긴 시간 동안 열리게 하여 활동전위에 의해 부호화되는 정보를 뒤섞어버림
- 전압개폐성 K+ 채널: 막이 탈분극되었을 때 열려 막전위를 음의 값으로 회복시킴
- 탈분극 이후 바로 열리지 않음 (1ms 정도의 지연 시간 존재 -> 지연성 전류기[delayed rectifier])
- 4개의 폴리펩타이드 소단위로 구성되어 있고, 이들이 모여 중간에 구멍을 형성함
- 막이 탈분극되면 소단위들은 구조적으로 변형되어 K+ 이온을 구멍으로 통과시킴
- 상대불응기: 전압개폐성 K+ 채널이 닫히기까지 막전위는 과분극됨
활동전위의 전도
- 정방향 전도(orthodromic conduction): 오직 한 방향으로만 전파되고 되돌아오지 않음 (활동전위가 이미 일어난 바로 뒷부분의 Na+는 비활성화되어 있음)
- 역방향 전도(antidromic conduction): 축삭의 어디에서든 활동전위는 탈분극에 의해 만들어질 수 있으므로 실험적으로 유도될 수 있음
- 전도 속도: 10m/s
- 한 지점에서 활동전위가 지속되는 시간은 약 2ms이기 때문에 활동전위가 진행되고 있는 막의 길이를 구할 수 있음
- 10m/s × 2 × 10-3s = 2cm
- 축삭에서 양전하가 빠져나가는 방법 (탈분극 후)
1. 축삭막을 통해 빠져나가는 방법 (축삭 지름 얇을 때)
2. 축삭을 따라 축삭 끝까지 전달되는 방법 (축삭 지름 두꺼울 때)
- 축삭이 두꺼울수록 더 먼 곳까지 탈분극시킬 수 있고, 결국 더 빠르게 활동전위 전도시킬 수 있음
- 따라서, 개체의 생존에 중요한 신경경로일수록 커다란 축삭을 가지고 있음 (e.g. 오징어의 거대축삭[회피반사에 관여])
- 크기가 작은 축삭일수록, 활동전위의 역치에 도달하기 위해 더 많은 탈분극이 필요하며 국소마취제에 더 민감함
- 척추동물은 주로 미엘린으로 축삭 속도 조절
- 국소마취제 조직에 직접 주사해 축삭의 활동전위를 일시적으로 차단하는 것
1. 점안마취(topical anesthesia): 젤 형태로 녹여 점막에 바르는 방법
2. 침윤마취(infiltration anesthesia): 조직에 직접 주사
3. 신경차단마취(nerve block): 신경에 직접 주사
4. 척수마취(spinal anesthesia): 뇌척수액(cerebrospinal fluid, CSF)에 주입하는 방법
- 코카인(cocaine): 임상적으로 최초로 도입된 국소마취제
- 리도카인(lidocaine): 현재 가장 광범위하게 사용되는 국소마취제
- 전압개폐성 Na+ 채널에 결합해 활동전위를 막음
- 리도카인의 결합 부위는 이 이온 채널의 IV번 도메인의 S6 alpha helix
- 리도카인은 세포 바깥에서 이 부위에 접근할 순 없고, 일단 축삭막을 넘어간 뒤 세포 안쪽에서 열린 이온채널로 들어가 결합함
- 탈미엘린성 질환(demyelinating disease)
- 도약전도가 파괴되어 반응시간에 심각한 지장 초래
1. 다발성 경화증(multiple sclerosis, MS)
- 축삭다발의 미엘린 수초를 공격하며, 공격받은 부위는 단단해지는 병변(lesion)이 생김 (이 경화증은 한 번에 신경계의 여러 군데를 공격)
2. 길랭-바레 증후군(Guillain-Barre syndrome)
- 근육과 피부를 자극하는 말초신경의 미엘린을 공격함
- 신경세포체와 수상돌기는 전압개폐성 Na+ 채널을 거의 갖고 있지 않고 주로 축삭에만 분포됨
- 따라서, 축삭둔덕(axon hillock)이 스파이크-개시구간(spike-initiation zone)이라고 불림
- 감각 뉴런에서 스파이크 개시구역은 감각신경종말(sensory nerve ending) 근처에 위치함
- 대뇌피질은 형태학적으로 가시 없는 성상세포와 가시 있는 피라미드세포로 나뉨
1. 성상세포(stellate cell)
- 일정한 탈분극 전류를 세포체에 가해주었을 때 자극이 있는 동안 일정한 간격을 갖는 활동전위를 발생시킴
2. 피라미드세포(pyramidal cell)
- 일정한 탈분극 전류를 세포체에 가해주었을 때 일정한 발화간격을 내지 못하고 점점 반응이 더뎌짐
- 자극이 가해질 때 반응속도가 느려지는 것을 적응이라 하고, 이는 흥분성 세포에 나타나는 성질
- 활동전위의 발화양식(firing pattern)은 짧은 휴지기간(pause) 후에 나타나는 빠른 활동전위들의 활동전위 폭발임
- 거대피라미드세포의 몇몇 아형을 포함한 어떤 세포들은 고정된 입련전류에 대해 율동적(rhytmic)이고 반복적인 활동전위 폭발로 반응함
'Biology > Neuroscience' 카테고리의 다른 글
| 신경과학 뇌의 탐구 - 5장 시냅스의 전달 (0) | 2024.10.25 |
|---|---|
| 신경과학 뇌의 탐구 - 3장 휴지 상태의 뉴런 세포막 (0) | 2024.06.28 |
| 신경과학 뇌의 탐구 - 2장 뉴런과 교세포 (0) | 2024.06.28 |
| 비침습적 뇌자극 (54) | 2023.08.18 |
| 뇌신경 (6) | 2023.05.07 |




댓글